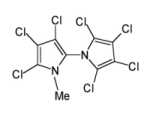
Abb.: Struktur des Naturstoffes Q1
Interessierte Leser seien an den Artikel in der Chemischem Rundschau, Nr. 4, 18.April 2006, S. 31-34 verwiesen
Unsere systematischen Untersuchungen zu diesem Thema setzten 1998 ein, als wir hohe Gehalte einer unbekannten und von uns als Q1 bezeichneten Organochlorverbindung in marinen Proben aus Afrika und der Antarktis nachwiesen (Mar. Poll. Bull. 38 (1999) 380-386). Von einer angereicherten Probe ergab sich bei der Untersuchung mit Hilfe der hochauflösenden Massenspektrometrie als exakte Masse 383,814 Da und damit die Summenformel C9H3Cl7N2 (Rapid Comm. Mass Spetrom. 21 (1999) 2118-2124). Bemerkenswerterweise war diese Summenformel in der Literatur für stabile Verbindungen bis dahin nicht bekannt. Q1 konnte in so unterschiedlichen Matrices wie Humanmilch und Luftproben nachgewiesen werden, und parallel dazu konnten wir zeigen, dass es sich bei Q1 um einen persistenten bioakkumulativen halogenierten Naturstoff handelt (Environ. Poll. 110 (2000) 401-409). Da Q1 in marinen Proben der südlichen Hemisphäre (Antarktis, südliches Afrika) stärker angereichert vorlag als in Proben der Nordhalbkugel (Mittel- und Nordeuropa, Nordamerika), lag es nahe, diesen Befund durch die Analyse von Proben aus Australien zu überprüfen. Bei dieser Zusammenarbeit mit Caroline Gaus und Jochen F. Müller (EnTox, Brisbane) wurden in Proben aus der Umgebung von Brisbane hohe Gehalte und im Fettgewebe eines Delphins mit 14 ppm (!) gar der bisher höchste Q1-Gehalt nachgewiesen (Arch. Environ. Contam. Toxicol. 41 (2001) 221-231, Chemosphere 46 (2002) 1477-1483).
Nach intensiven massenspektrometrischen Untersuchungen erhärtete sich der Verdacht, dass Q1 ein Bipyrrol-Grundgerüst zugrunde liegt. Durch gezielte Synthese konnte Q1 in unserer Arbeitsgruppe schließlich in Grammmengen synthetisiert und dabei seine Struktur als 2,3,3´,4,4´,5,5´-Heptachlor-1´-Methyl-1,2´-Bipyrrol aufgeklärt werden:

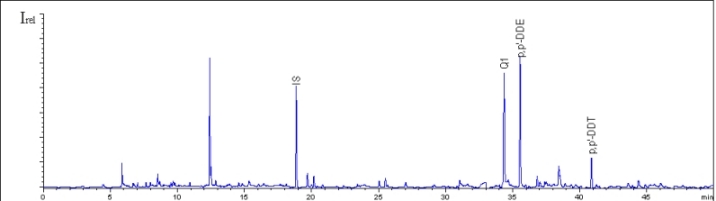
In den australischen Proben fielen uns neben Q1 aber noch andere intensive Signale auf, die zunächst als Organobromverbindungen identifiziert wurden (Arch. Environ. Contam. Toxicol. 41 (2001) 221-231). Der Verdacht, dass es sich dabei um halogenierte Naturstoffe handeln könnte, erhärtete sich schnell, denn mehrere bromierte Naturstoffe waren in der gleichen Region von Naturstoffchemikern um Mary Garson (University of Queensland, Brisbane) beschrieben worden. Durch Probenaustausch konnten wir zeigen, dass zwei der wichtigsten halogenierten Naturstoffe in unseren Proben von Schwämmen produziert werden, und damit konnten wir auch BC-2 als 4,6-Dibrom-2-(2´,4´-dibrom)phenoxyanisol und BC-11 als 3,5-Dibrom-2-(3´,5´-dibrom, 2´-methoxy)phenoxyanisol identifizieren (Environ. Toxicol. Chem. 21 (2002) 2014-2019).
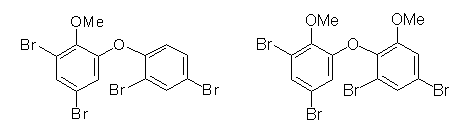
Interessant ist, dass sich die beiden o. g. bromierten Naturstoffe nur durch eine oder zwei Methoxygruppen von den als äußerst toxisch eingestuften bromierten Diphenylethern (BDEs), die anthropogener Herkunft sind und im Flammschutz eingesetzt werden, unterscheiden (BILD). Gerade erst wurde das so genannte Pentabrom-Gemisch von der EU verboten. Dabei sind die von uns bestimmten höchsten Gehalte an bromierten Naturstoffen (ΣBCs >5 mg/kg Fett) gleich hoch wie die jemals in Lebensmittel- und Umweltproben bestimmten Gehalte der toxischen BDEs (Environ. Toxicol. Chem. 21 (2002) 2014-2019). Somit gilt zu klären, ob auch die halogenierten Naturstoffe eine ähnliche Toxizität aufweisen und ob ggf. zum Schutze des Verbrauchers Grenzwerte für Lebensmittel etabliert werden sollten.
Kürzlich wurden von uns mehrere Tribromphenoxyanisole in marinen Organismen nachgewiesen, von denen einige bisher nicht von Naturstoffchemikern beschrieben worden waren (Environ. Sci. Technol. 39 (2005) 7784). Einige dieser Verbindungen wiesen ein Substitutionsmuster auf, dass darauf schließen lässt, dass es sich dabei um Metabolite der Tetrabromphenoxyanisole handelt (Environ. Sci. Technol. 39 (2005) 7784).
Das bereits erwähnte BC-2 wurde von uns synthetisiert (Chemosphere 52 (2003) 423-431) und - wie auch Q1 - kommerziell zugänglich gemacht (Standards der von uns synthetisierten Naturstoffe Q1 und BC-2 können bei LGC Promochem (Wesel) für die quantitative Analyse bezogen werden.=>Bestellnummern)
Mit MHC-1 (mixed halogenated compound) konnte in Zusammenarbeit mit Josef Hiebl vom Landesuntersuchungsamt für das Gesundheitswesen Südbayern in Oberschleißheim ein weiterer bedeutender Naturstoff genauer beschrieben werden. Dieser hatte in Fischen aus der Lebensmittelüberwachung eine auffällige Verbindung entdeckt und war - aufgrund unserer Arbeiten über Q1 - mit uns in Kontakt getreten. Wieder wurde die Summenformel von MHC-1 mittels hochauflösender MS als C10H13Br2Cl3 ermittelt. Somit handelt es sich aller Wahrscheinlichkeit nach um ein gemischthalogeniertes Monoterpen (Environ. Sci. Technol. 35 (2001) 4157-4162). MHC-1 lag in Fischproben aus der Lebensmittelüberwachung (Seelachs) mit Gehalten von bis zu 0,9 mg/kg vor und konnte bisher in Proben aus vier Kontinenten nachgewiesen werden.
Kürzlich konnte von uns in Zusammenarbeit mit Kollegen aus der Lebensmittelüberwachung (Josef Hiebl, Oberschleißheim) eine neue Klasse von Naturstoffen nachgewiesen werden, die insbesondere in kommerziellen Fischproben aus dem Mittelmeer vorzufinden sind (J. Agric. Food Chem. 54 (2006) 2652-2657). Dabei handelt es sich um erstmals von Mary Garson und Mitarbeitern in australischen Flachwasserschwämmen nachgewiesene Verbindungen (Abb.).
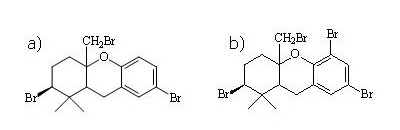
Durch die ufernahe Ansiedlung von Fischfarmen verbunden mit dem höheren Fettgehalt von Zuchtfischen, kommt es zu einem verstärkten Auftreten dieser Stoffe in marinen Lebensmitteln. Eine ständige und intensive Kontrolle sollte daher aus unserer Sicht durchgeführt werden, um den Verbraucher vor unerwünschten und vermeidbaren Belastungen zu schützen.
Der Nachweis halogenierter Naturstoffe erfolgt am besten mit Hilfe einer von uns entwickelten GC/NCI-MS-Methode (Anal. Chem 73 (2001) 4951-4957), die in der Folge weiter verfeinert wurde (Fresenius Environ. Bull. 11 (2002) 170-175).
Mit dieser hochempfindlichen Methode wurden inzwischen viele weitere potentielle Naturstoffe mariner Herkunft in Lebensmitteln entdeckt (Eur. Food Res. Technol. 215 (2002) 523-528; Chemosphere 52 (2003) 415-422; Chemosphere 52 (2003) 423-431). Zu den häufig in marinen Lebensmitteln detektierten Verbindungen zählt z. B. auch 2,4,6-Tribromanisol (TBA), für das es neben natürlichen auch anthropogene Quellen gibt.
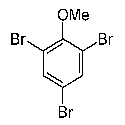
Allerdings entsteht TBA in der Natur leicht aus Tribromphenol, das eine wichtige Aromakomponente in Meerestieren (z. B. Seefisch und Shrimps) ist. TBA wurde von uns in Zusammenarbeit mit Martin Schlabach und Roland Kallenborn vom Norwegian Institute for Air Research (NILU) als wichtigste bromhaltige Verbindung in Luftproben der Arktis und Antarktis identifiziert (Fresenius Environ. Bull. 11 (2002) 170-175).
Unsere gegenwärtigen Untersuchungen zielen auf